Fondé en 1974, le Centre d’Études et de Recherche sur le Médicament de Normandie · CERMN · est une Unité de Recherche de l’université de Caen Normandie développant des programmes de recherche dans le domaine du Drug Design. Elle occupe depuis janvier 2009 des locaux sur le campus du Pôle de Formation et de Recherche en Santé · PFRS · de l’université de Caen Normandie, à proximité immédiate du CHU de Caen Normandie, du CLCC Baclesse, du Centre CYCERON.
Direction

Organigramme
Groupes
Les activités de recherche au sein du groupe sont basées sur l’analyse de données en chémoinformatique avec l’intégration de données internes (chimiothèque du CERMN) et externe (bases publiques) et l’analyse des interactions ligands-récepteurs. Le but est de comprendre les relations structures-activités et de concevoir de nouveaux ligands d’intérêts biologiques.
Data Mining en chémoinformatique
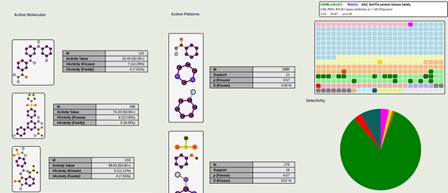
Nos premiers travaux dans le domaine du data mining ont été initiés dans le cadre du programme Minomics · CERMN / GREYC. Celui-ci reprend les technologies basées sur la notion de contraste. L’objectif est de comprendre l’accord entre un profil d’activité polypharmacologie ici et des motifs chimiques présents sur les structures. Cette analyse, accompagnée d’un développement logiciel, se réalise au niveau 2D avec une intégration des distances et un raisonnement pharmacophorique. Ces techniques sont un prolongement des méthodes d’analyse comparative des pharmacophores à l’origine des ligands 5-HT du laboratoire.
À titre d’illustration · Dr J.P. Métivier / Dr A. Lepailleur / Pr R. Bureau, une étude préliminaire concerne les kinases GSK-PKIS pour les données sur ChEMBL avec une analyse 2D des motifs actifs sur une famille ainsi que leurs correspondances sur l’ensemble des kinases. L’illustration présentée ci-dessus n’intègre pas les distances.
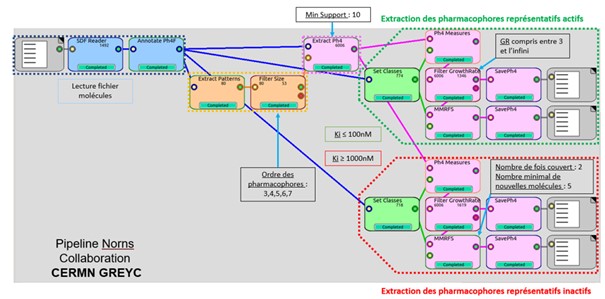
Un programme type workflow nommé Norns (voir illustration ci-dessous), en lien avec MinoMics, a été élaboré. Une illustration, de son application, sur des ligands d’une tyrosine kinase BCR-ABL est décrite dans une publication de 2018 (J. Med. Chem).
Conceptions basées sur les complexes ligands-récepteurs.
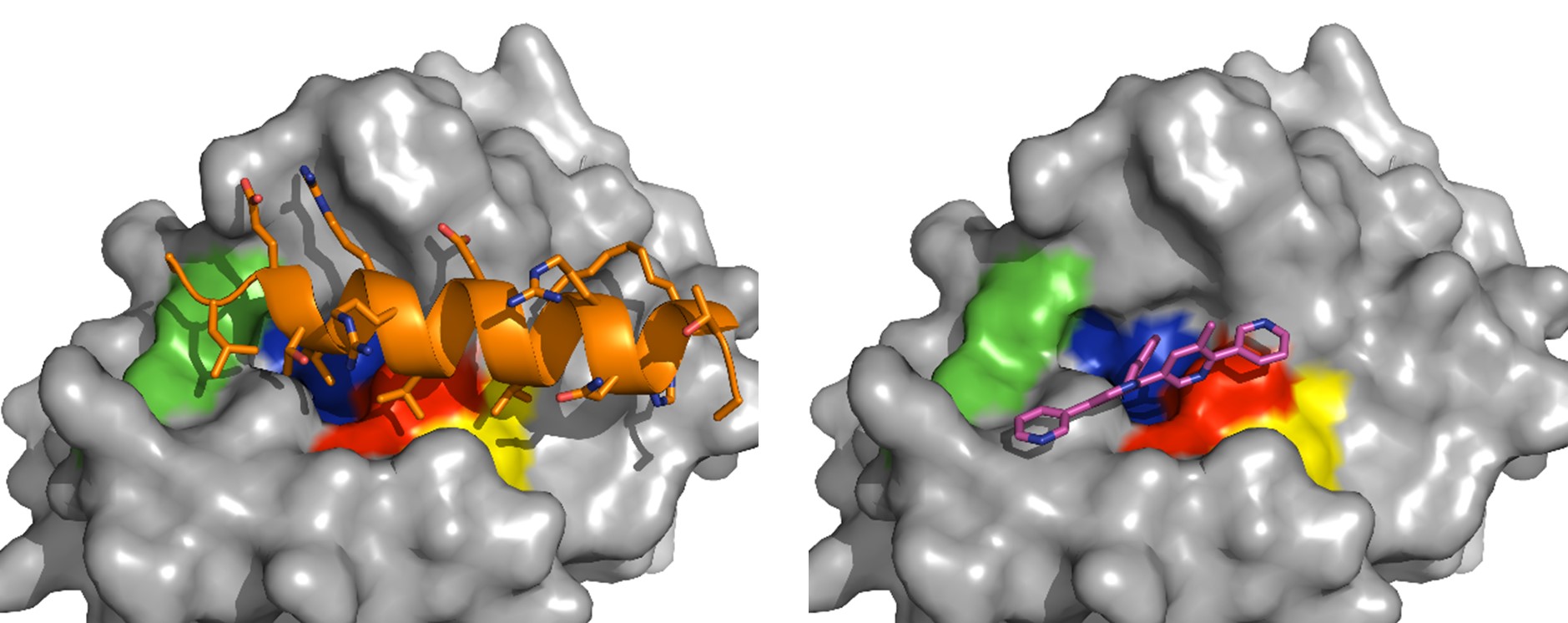
Nous réalisons des simulations de docking, nous permettant de prédire un positionnement ponctuel des ligands dans le site actif des cibles d’intérêt. Suite à cela, nous réalisons des simulations de dynamique moléculaire pour estimer l’énergie libre de liaison du ligand avec sa cible (ΔGliaison). Ces techniques ont été appliquées avec succès à la conception de Pyridoclax, une molécule antiproliférative prometteuse (brevet).
Dans le but d’apporter plus d’informations sur la dynamique de formation des complexes ligand-cible et ainsi pouvoir orienter plus finement les pharmacomodulations, nous développons également d’autres protocoles :
- un protocole de simulation permettant d’analyser de manière théorique les aspects thermodynamiques et cinétiques associés à la formation des complexes ligand-cible (prédiction de kon et koff).
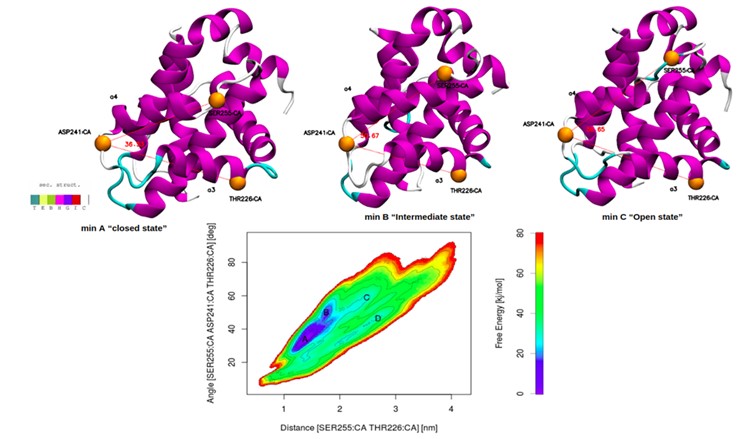
- des protocoles de simulation de métadynamique pour estimer la variation de l’énergie libre entre différents états conformationnels de protéines, que nous souhaitons élargir vers les systèmes complexés aux ligands.
Ces activités de recherche sont intégrées aux adressages thématiques de l’unité et peuvent faire l’objet de collaborations et de prestations externes via la plateforme Drug Design du CERMN.
Le Groupe Chimie Thérapeutique s’intéresse au Drug Design en utilisant des méthodes telles que la fouille de chimiothèques (Structure-Based Drug Design, Ligand-Based Drug Design) ou des approches par fragments (Fragment-Based Drug Design), tout en développant de nouvelles méthodologies de synthèse (chimie hétérocyclique, réactions métallocatalysées, garlanding de foldamères abiotiques…).
L’utilisation de cette expertise a conduit les activités de recherche du groupe vers la conception de foldamères, de modulateurs des RCPGs et de prodrogues pléiotropiques, mais également vers le développement de l’approche PROTAC (PROteolysis Targeting Chimera). Dans nos projets, ces résultats nous engagent dans une stratégie Hit-to-Lead Chemistry puis dans des opérations de Lead optimization.
Les activités du groupe concernent également le repositionnement de molécules actives via une stratégie innovante. Le repositionnement de principes actifs, à l’origine de près d’un quart des revenus de l’industrie pharmaceutique est actuellement en plein essor. Dans cette optique, afin de rationaliser la découverte de nouveaux candidats médicaments, nous avons initié une collaboration avec le centre de pharmacovigilance du CHU de Caen. L’approche PROTAC est quand à elle utilisée pour valoriser les composés qui sont rejetés au cours du développement de candidats médicaments en raison d’un manque d’activité pharmacologique ou de sélectivité pour le tissus visé.
Ces projets s’intègrent plus largement dans des programmes de recherche coopératifs, pluridisciplinaires, mettant en synergie les savoir-faire les plus récents des équipes de recherche et ceci au moyen d’une stratégie totalement intégrée associant chimie médicinale, analyse structurale, chémoinformatique, évaluation de la pharmacopotentialité et des paramètres PK/PD et évaluation biologique.
Ces activités de recherche sont intégrées aux adressages thématiques de l’unité et peuvent faire l’objet de collaborations et de prestations externes via la plateforme Drug Design du CERMN.
Les activités de recherche du groupe Formulation s’inscrivent dans le prolongement de celles proposées précédemment par la plateforme Screening & Drugabilité du CERMN (plan quinquennal 2017-2021).
Ainsi, les membres de ce groupe développent des formulations galéniques innovantes intégrées au drug discovery. Des nanovecteurs passifs ou actifs – de type nanoémulsions, nanoparticules, liposomes, associés, si nécessaire, à des gels thermosensibles et/ou mucoadhésifs – sont développés en vue d’améliorer la solubilité relative et/ou d’optimiser la biodistribution de leads identifiés ou de substances actives repositionnées.
Ces nanoformulations sont d’emblée conçues pour être polyvalentes et adaptées à de multiples voies d’administration (orale, intraveineuse, nasale).
Elles sont caractérisées d’un point de vue physico-chimique, pharmacotechnique et biopharmaceutique pour être sûres d’utilisation afin d’en garantir l’efficacité thérapeutique et/ou diagnostique et ainsi contribuer au développement d’un médicament.
Elles trouvent leurs applications thérapeutiques dans le domaine des neurosciences (traitement de la maladie d’Alzheimer, inflammation du cerveau) et/ou de cancers (cancer de l’ovaire, lymphome, glioblastome) ou d’autres pathologies à sombre pronostic pour lesquelles les nanoformulations offrent de nouvelles perspectives de guérison.
En amont de ces développements, en utilisant des tests miniaturisés et peu consommateurs de produits, les caractéristiques physico-chimiques (solubilité, logP, passage de barrières digestive et hématoencéphalique, interactions membranaires, stabilité…), susceptibles d’impacter le devenir et l’efficacité in vivo de molécules, sont également déterminés.
En parallèle, du fait de ses compétences transversales et complémentaires, le groupe Formulation développe des tests in vitro afin d’évaluer de façon précoce l’activité de nouveaux composés par rapport à des cibles biologiques d’intérêt pour l’unité (cholinestérases, peptide amyloïde, récepteurs sérotoninergiques, activités antioxydante et chélatante métallique,…).
Ces activités de recherche sont intégrées aux adressages thématiques de l’unité et peuvent faire l’objet de collaborations et de prestations externes via la plateforme Drug Design du CERMN.
Les activités de recherche au sein du groupe « méthodologie de synthèse et radiochimie » sont principalement centrées sur le développement de nouvelles méthodes de synthèse en radiochimie, en chimie Host-Guest et leurs applications pour le développement d’agents de contraste en imagerie.
En radiochimie, nous développons des méthodes de radio-iodation innovantes en chimie organométallique à l’aide de métaux comme le palladium, l’or ou le cobalt utilisant de l’iode-125 au sein de la plate-forme IMOGERE de l’université de Caen. Nous sommes par ailleurs équipés du matériel nécessaire à l’utilisation d’iode-123 dans le cadre d’une collaboration avec le service de médecine nucléaire du CHU de Caen. Les méthodes développées au sein du groupe sont transposées à d’autres isotopes radioactifs (18F, 11C, 14C, 3H et 211At) en collaboration avec d’autres équipes (SHFJ, SCBM, HUG). Les nouvelles méthodes de radio-iodation développées sont également mises à profit pour la synthèse de radiotraceurs pour l’imagerie SPECT (Single Photon Emission Computed Tomography) et PET (Positron Emission Tomography).
Dans le domaine de la chimie Host-Guest, nous développons de nouvelles méthodes de synthèse de cyclotrivératrilènes et de cryptophanes originaux, de symétrie C1 et/ou C3 hydrosolubles afin de les utiliser comme biosondes à Xe hyperpolarisé en imagerie IRM. Cette thématique a été développée au sein du projet NanoXe_Inflammation (chaire d’excellence régionale), puis dans le cadre du projet CrIM (maturation Normandie Valorisation) en collaboration avec le groupe formulation du CERMN, le laboratoire PhIND et le LCS.
Ces activités de recherche sont intégrées aux adressages thématiques de l’unité et peuvent faire l’objet de collaborations et de prestations externes via la plateforme Drug Design du CERMN.
Personnel